Stickstoffkreislauf einfach erklärt
Stickstoff ist entscheidend für Aminosäuren und DNA. Erfahre, wie der Stickstoffkreislauf in vier Schritten abläuft – von der Fixierung bis zur Denitrifikation. Beteilige dich an Beispielen aus verschiedenen Ökosystemen und verstehe, warum der menschliche Einfluss wichtig ist. Dies und mehr findest du im folgenden Text!
Inhaltsverzeichnis zum Thema Stickstoffkreislauf
Das Quiz zum Thema: Stickstoffkreislauf
Was passiert bei der Stickstofffixierung im Stickstoffkreislauf?
Frage 1 von 5
Welcher Schritt im Stickstoffkreislauf beschreibt die Umwandlung von Ammonium zu Nitrat?
Frage 2 von 5
Was beinhaltet der Stickstoffkreislauf nicht?
Frage 3 von 5
Welche Rolle spielen Destruenten im Stickstoffkreislauf?
Frage 4 von 5
Was kann passieren, wenn der Stickstoffkreislauf durch den Menschen gestört wird?
Frage 5 von 5
Wie willst du heute lernen?
Stickstoffkreislauf – Definition
Stickstoff ist ein chemisches Element mit dem Symbol N. Es kommt in der Natur in verschiedenen Formen vor. In der Luft kommt Stickstoff hauptsächlich in molekularer Form als N2 vor oder aber in stickstoffhaltigen Gasen wie Stickoxiden und Ammoniak. Stickstoff ist ein wichtiger Bestandteil von Aminosäuren und damit in allen Proteinen enthalten und auch unsere Erbinformation, die DNA, enthält Stickstoff. Pflanzen benötigen Stickstoff als Nährstoff und auch wir Menschen müssen Stickstoff aufnehmen.
Der Stickstoffkreislauf beschreibt den Transport und die stetige Umwandlung von gasförmigem Stickstoff aus der Luft in anorganische und organische Stickstoffverbindungen sowie die schrittweise Rückführung in die Umwelt.
Stickstoffkreislauf – Ablauf
Der Stickstoffkreislauf läuft in mehreren Schritten ab, die wir uns im Folgenden genauer ansehen werden.
Stickstofffixierung
Die Stickstofffixierung ist der erste und grundlegende Schritt im Stickstoffkreislauf. Dabei wird molekularer Stickstoff (N2) aus der Atmosphäre gebunden. Der elementare Stickstoff wird gespalten und in Verbindungen, die von Pflanzen und anderen Lebewesen genutzt werden können, umgewandelt.
Dazu sind beispielsweise stickstofffixierende Bakterien, wie die Knöllchenbakterien, in der Lage. Sie leben im Boden in Symbiose mit bestimmten Pflanzen und wandeln molekularen Stickstoff (N2) in Ammoniak (NH3) oder Ammoniumionen (NH4+) um. Den umgewandelten Stickstoff geben sie an Pflanzen weiter, die ihn für das Wachstum benötigen.
Auch durch abiotische Faktoren kann Stickstoff fixiert werden. Durch Sonneneinstrahlung oder Blitzeinschläge kann der elementare Luftstickstoff zu Ammoniak (NH3) oder Ammoniumionen (NH4+) reagieren.
Eine technische Möglichkeit, um elementaren Stickstoff zu fixieren, ist das Haber-Bosch-Verfahren. Dadurch kann aus dem Luftstickstoff Ammoniak hergestellt werden, beispielsweise zur Verwendung in stickstoffhaltigen Düngemitteln.
Nitrifikation
Ammoniak kann in zwei Schritten zu Nitrat (NO3–) umgewandelt werden. Bestimmte Bakterien, die Nitrifizierer, können Ammoniumionen oder Ammoniak zu Nitrit (NO2–) oder zu Nitrat (NO3–) umwandeln. Dies ist günstig für die Pflanzen, da sie Stickstoff bevorzugt in Form von Nitrat aufnehmen. In den Pflanzen wird Stickstoff in Proteine eingebaut. Wenn andere Lebewesen die Pflanzen essen, nehmen sie dadurch auch den benötigten Stickstoff auf.
Für die Reaktion sind aerobe (sauerstoffreiche) Bedingungen erforderlich.
Ammonifikation
Ein Teil des von den Lebewesen aufgenommenen Stickstoffs wird in Form von Urin und Kot an die Umwelt abgegeben. Auch abgestorbene Pflanzen und Tiere enthalten Stickstoffverbindungen. Die Ausscheidungen und das tote Material werden zerkleinert. Destruenten wie Pilze und Bakterien können den Stickstoff aus dem zerkleinerten organischen Material in Ammoniak oder Ammoniumionen umwandeln. Der Ammoniak und die Ammoniumionen stehen nun wieder für andere Lebewesen wie nitrifizierende Bakterien zur Verfügung, die ihn in für Pflanzen verfügbares Nitrat umwandeln können.
Denitrifikation
Bei der Denitrifikation wird Nitrat durch denitrifizierende Bakterien in elementaren Stickstoff (N2) umgewandelt. Dazu sind anaerobe Bedingungen erforderlich (ohne Sauerstoff). Die gasförmigen Stickstoffverbindungen werden der Luft zugeführt und der Stickstoffkreislauf schließt sich. Die Denitrifikation wird auch als Nitratatmung bezeichnet, da es eine Form der anaeroben Atmung ist.
Die Tabelle fasst die vereinfachten Reaktionsgleichungen der Nitrifikation und die Formeln der Denitrifikation zusammen.
| Schritt | Reaktionsgleichung |
|---|---|
| Nitrifikation | NH4+ → NO2– → NO3– oder NH3 + 2 O2 → NO3– + H+ + H2O |
| Denitrifikation | NO3– → NO2– → NO + N2O → N2 |
Stickstoffkreislauf – Beispiele
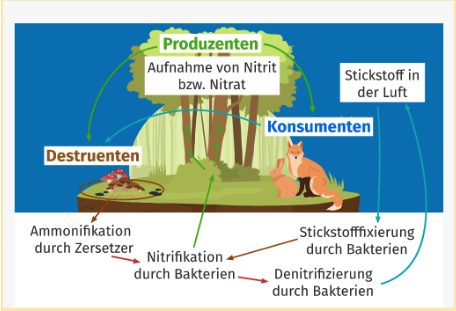
Am Stickstoffkreislauf in der Natur sind sowohl Produzenten, Konsumenten als auch Destruenten beteiligt. Die Produzenten sind beispielsweise Pflanzen, Konsumenten sind die Lebewesen, die die Pflanzen oder andere Konsumenten fressen, und Destruenten sind Zersetzer wie Pilze und Bakterien, die Abfallstoffe und totes organisches Material abbauen. Sie können in verschiedenen Ökosystemen am Stickstoffkreislauf beteiligt sein.
In der Abbildung siehst du das Schema eines Stickstoffkreislaufs am Beispiel Ökosystem Wald.
Stickstoffkreislauf in Gewässern
Die Stickstofffixierung erfolgt in stehenden und fließenden Gewässern durch Cyanobakterien. Sie fixieren den Luftstickstoff und produzieren Ammonium. Durch bestimmte Bakterien erfolgt anschließend die Nitrifizierung, also die Umwandlung des Ammoniums zu Nitrit und Nitrat.
Die Produzenten in Gewässern sind Wasserpflanzen, Plankton und Algen. Sie betreiben Fotosynthese und bauen Biomasse auf. Dafür benötigen sie unter anderem Stickstoff, den sie in Form von Ammonium, Nitrat oder Nitrit aufnehmen.
Konsumenten im Ökosystem See sind beispielsweise Fische, Wasservögel und Krebse. Diese nehmen Stickstoffverbindungen auf, indem sie Pflanzen oder andere Tiere essen.
Sterben die Produzenten oder Konsumenten ab, werden sie durch Destruenten wie Bakterien und Würmer zersetzt und der enthaltene Stickstoff wird während der Ammonifikation in Form von Ammonium freigesetzt.
Der Prozess der Ammonifikation verbraucht viel Sauerstoff. Wenn viel organisches Material vorhanden ist, das durch Destruenten zersetzt werden muss, kann es zu einer Sauerstoffknappheit im Gewässer kommen. Dies geschieht vor allem in stehenden Gewässern und kann auch in Aquarien zum Problem werden. Außerdem wird der pH-Wert durch die hohen Gehalte an Ammonium angehoben. Ein zu hoher pH-Wert gefährdet das Ökosystem.
Häufig gestellte Fragen zum Thema Stickstoffkreislauf









Alle Artikel aus dem Fach Biologie