RGT-Regel – Definition und Beispiele
Die RGT-Regel, auch als Reaktionsgeschwindigkeit-Temperatur-Regel bekannt, besagt, dass sich die Reaktionsgeschwindigkeit verdoppelt bis vervierfacht, wenn die Temperatur um 10 °C steigt. Entdecke, wie diese Regel in der Chemie und Biologie, insbesondere bei Enzymen, angewendet wird. Dies und vieles mehr findest du im folgenden Text.
Inhaltsverzeichnis zum Thema RGT-Regel
Wie willst du heute lernen?
RGT-Regel – Definition
Die RGT-Regel stellt eine Verbindung zwischen der Temperatur und der Reaktionsgeschwindigkeit her. Die RGT-Regel besagt, dass sich bei einer Temperaturerhöhung um 10 °C bzw. 10 K die Reaktionsgeschwindigkeit ungefähr verdoppelt bis vervierfacht. Dieser Zusammenhang kann mithilfe des Van’t-Hoff-Gesetzes berechnet werden. Mithilfe dieser Formel wird der sogenannte Q10-Faktor berechnet. Der Q10-Wert gibt die Beschleunigung der Reaktionsgeschwindigkeit an, wenn die Temperatur um 10 K steigt.
RGT-Regel – Kollisionsmodell
Stellt man sich Atome und Moleküle als kleine Kugeln vor, sind diese nicht starr, sondern bewegen sich mit einer bestimmten Geschwindigkeit in einem Medium, z. B. Luft oder Flüssigkeit. Kommt es aufgrund dieser zufällig ausgerichteten Bewegungen zu einer Kollision zweier Teilchen, können diese miteinander reagieren. Nach der Stoßtheorie der Chemie ist eine chemische Reaktion definiert als das Zusammenstoßen von Teilchen. Eine Reaktion findet nur statt, wenn bei einem Zusammenstoß eine bestimmte Energie, die sogenannte Aktivierungsenergie, erreicht wird. Nicht immer führt die Kollision von zwei Teilchen also zu einer Reaktion. Wird die Temperatur erhöht, vergrößert sich auch die Geschwindigkeit der Atome und Moleküle. Die Möglichkeit einer Kollision wird größer und auch die kinetische Energie der Teilchen ist höher. Beide Faktoren erhöhen die Wahrscheinlichkeit einer Reaktion bei einem Zusammenstoß zweier Teilchen. Neben der kinetischen Energie spielt auch der Stoßwinkel eine Rolle bei der Frage, ob eine Reaktion stattfindet oder nicht.
RGT-Regel – Enzyme
Auch im Stoffwechsel von Organismen gilt die RGT-Regel. Stoffwechselprozesse laufen bei höheren Temperaturen schneller ab, da Enzyme und Substrate schneller miteinander reagieren können. Die Enzymaktivität steigt also mit zunehmender Temperatur. Allerdings ist zu beachten, dass Enzyme ein spezifisches Temperaturoptimum besitzen, also die Temperatur, bei der sie am schnellsten Substrate umsetzen können.
Außerdem unterliegt die RGT-Regel bei physiologischen Prozessen einem Temperaturlimit. Stoffwechsel findet in der Regel nur in einem Temperaturbereich von 1 °C bis 37 °C. Unterhalb dieser Temperaturen gefriert Wasser, oberhalb denaturieren Proteine und damit auch Enzyme.
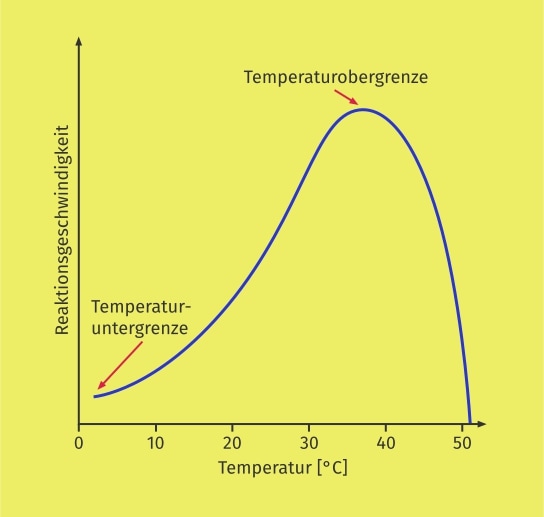
Die Abbildung zeigt die Zunahme der Reaktionsgeschwindigkeit in Abhängigkeit von der Temperatur innerhalb der Temperaturober- und -untergrenze für Enzyme.
RGT-Regel – Anwendung
Der Q10-Faktor, der den Wert für die Reaktionsbeschleunigung angibt, kann mit folgender Formel berechnet werden:
![]()
| Wert | Erläuterung |
|---|---|
| k1 und k2 | Reaktionsgeschwindigkeitskonstanten der an der Reaktion beteiligten Stoffe |
| T1 und T2 | die unterschiedlichen Temperaturen, unter denen diese Reaktion abläuft |
Mit dieser Formel lässt sich die Beschleunigung einer Reaktion auf Grundlage der RGT-Regel mit Rechenbeispielen bestimmen.
Häufig gestellte Fragen zum Thema RGT-Regel









Alle Artikel aus dem Fach Chemie