Aggregatzustände einfach erklärt – Definition, Bedeutung und Beispiele
Erfahre, wie feste, flüssige und gasförmige Zustände definiert sind und wie sie sich durch Temperatur- oder Druckänderungen ändern. Tauche ein in das Teilchenmodell und entdecke, wie sich die Wechselwirkungen zwischen den Teilchen je nach Aggregatzustand unterscheiden. Dies und mehr erwarten dich im folgenden Text!
Inhaltsverzeichnis zum Thema Aggregatzustände
Das Quiz zum Thema: Aggregatzustände
Was beschreibt der Begriff Aggregatzustand?
Frage 1 von 5
Wie viele klassische Aggregatzustände gibt es?
Frage 2 von 5
Was ist charakteristisch für den festen Aggregatzustand im Teilchenmodell?
Frage 3 von 5
Wie nennt man den Übergang von flüssig zu gasförmig?
Frage 4 von 5
Welcher Phasenübergang bezeichnet den Übergang von gasförmig zu fest?
Frage 5 von 5
Wie willst du heute lernen?
Aggregatzustände – Definition
Der physikalische Zustand eines Stoffes wird durch den Aggregatzustand beschrieben. Wir unterscheiden in der klassischen Physik die drei Aggregatzustände fest, flüssig und gasförmig. Welchen Zustand ein Stoff annimmt, hängt vom Stoff selbst, der Temperatur sowie dem Druck und dem eingenommenen Volumen ab.
Die verschiedenen Eigenschaften der drei Aggregatzustände (fest, flüssig und gasförmig) sind in der folgenden Tabelle zusammengefasst.
| Aggregatzustand | Eigenschaft |
|---|---|
| fest | feste Form, bestimmtes Volumen |
| flüssig | keine feste Form, bestimmtes Volumen |
| gasförmig | keine feste Form, kein bestimmtes Volumen |
Ein fester Stoff lässt sich aufgrund seiner festen Form und seines definierten Volumens schwer verformen. Ein flüssiger Stoff hingegen nimmt die Form seines Gefäßes an, das Volumen bleibt jedoch gleich. Ein gasförmiger Stoff breitet sich in dem ihm zur Verfügung stehenden Raum aus, sein Volumen ist variabel.
Jeder Stoff kann in den drei Zuständen fest, flüssig und gasförmig vorkommen und auch zwischen den Aggregatzuständen wechseln. Dafür ist zum Beispiel eine Temperatur- oder Druckänderung nötig.
Aggregatzustände im Teilchenmodell
Das Teilchenmodell ist Grundlage vieler physikalischer Prozesse. Es besagt, dass alle Stoffe aus kleinen Teilchen (Molekülen oder Atomen) bestehen, die sich nicht weiter teilen lassen, ohne den Stoff zu zerstören. Die kleinsten Teilchen unterscheiden sich je nach Stoff. Sie sind zudem ständig in Bewegung. Wie schnell sie sich bewegen, hängt von der Temperatur des Stoffes ab. Die Kräfte zwischen den Teilchen sorgen dafür, dass der Stoff nicht auseinanderfällt. Je nach Aggregatzustand eines Stoffes ist auch die Wechselwirkung zwischen den Teilchen unterschiedlich.
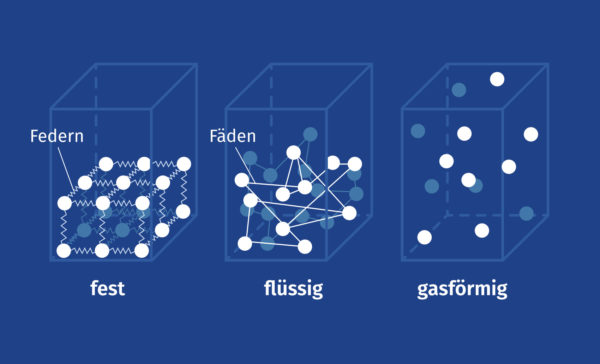
Teilchenmodell – fester Aggregatzustand
Die starken Anziehungskräfte im festen Zustand sorgen dafür, dass die Teilchen sich an einem festen Ort befinden und sich nur minimal bewegen. Zudem sind die Abstände zwischen ihnen sehr klein.
Teilchenmodell – flüssiger Aggregatzustand
Bei flüssigen Stoffen ist die Anziehungskraft zwischen den Teilchen geringer als bei festen Stoffen. Auch der Abstand zwischen den Teilchen ist größer. Die Teilchen können sich recht frei bewegen, haben also keinen festen Platz. Die Anziehung ist jedoch immer noch so groß, dass flüssige Stoffe ein bestimmtes Volumen besitzen, weshalb man auch von einer relativ freien Bewegung spricht.
Teilchenmodell – gasförmiger Aggregatzustand
Die Anziehungskraft zwischen den Teilchen im gasförmigen Stoff ist kaum noch vorhanden. Die Teilchen bewegen sich sehr frei und mit großen Abständen zueinander. Somit kann sich das Volumen des Stoffes verändern, je nachdem wie viel Raum ihnen zur Verfügung steht.
Änderung der Aggregatzustände
Mithilfe des Teilchenmodells lässt sich leichter verstehen, warum sich der Aggregatzustand eines Stoffes ändert. Die Bewegung der Teilchen hängt von der Temperatur eines Stoffes ab. Je höher die Temperatur, desto stärker die Teilchenbewegung. Somit zeigt sich, dass eine Änderung der Temperatur auch zu einer Änderung des Aggregatzustands führen kann.
Phasenübergänge
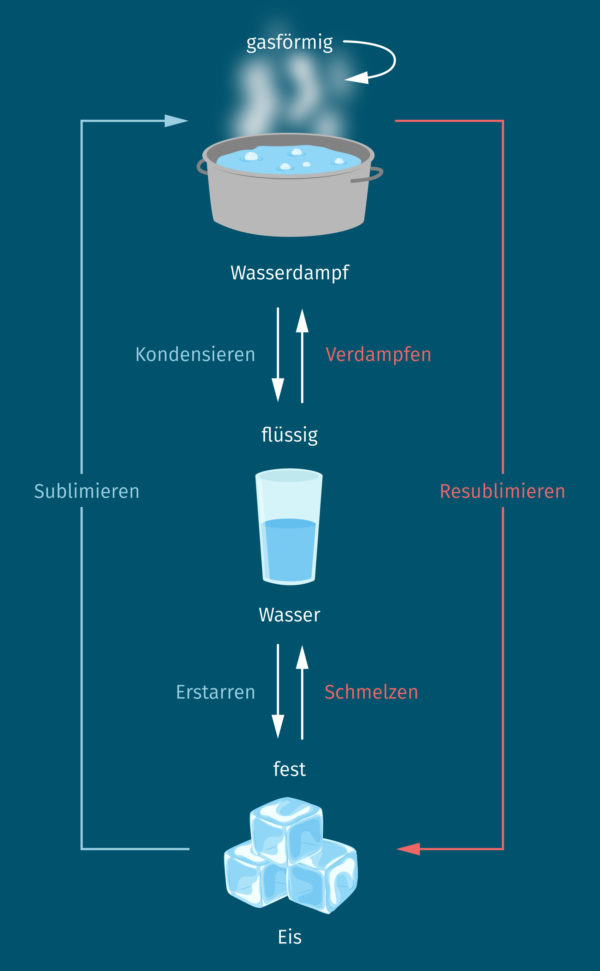
Der Übergang von einem in einen anderen Aggregatzustand wird Phasenübergang genannt. Jeder Phasenübergang hat seine besondere Bezeichnung.
- Übergang von fest zu flüssig: Schmelzen
- Übergang von flüssig zu fest: Erstarren
- Übergang von flüssig zu gasförmig: Verdampfen
- Übergang von gasförmig zu flüssig: Kondensieren
- Übergang von fest zu gasförmig: Sublimieren
- Übergang von gasförmig zu fest: Resublimieren
Beachte: Auch wenn sich das Aussehen und die Eigenschaften eines Stoffes beim Phasenübergang verändern, bleibt er chemisch gesehen gleich. Der Stoff besteht weiterhin aus den gleichen Teilchen.
Änderungen der Aggregatzustände am Beispiel von Wasser
Viele Stoffe kommen in unserem Alltag nur in einem oder maximal zwei Aggregatzuständen vor. Anders ist das jedoch bei Wasser. Dieses wird deshalb häufig als Beispiel zur Beschreibung der verschiedenen Aggregatzustände und Phasenübergänge genutzt.
Die Zustandsformen von Wasser sind:
- Eis/festes Wasser (fester Aggregatzustand)
- Flüssiges Wasser (flüssiger Aggregatzustand)
- Wasserdampf (gasförmiger Aggregatzustand)
Da auf der Erdoberfläche der Druck relativ konstant ist, betrachten wir die Phasenübergänge von Wasser im folgenden Beispiel anhand der Temperaturänderung.
Der Übergang von fest zu flüssig wird als Schmelzen bezeichnet. Ein fester Stoff schmilzt beim Erreichen einer bestimmten Temperatur, der sogenannten Schmelztemperatur. Diese wird durch die Zufuhr von Wärme erreicht.
Die sogenannte Schmelztemperatur von Wasser liegt (bei einem Normaldruck von rund ![]() ) bei
) bei ![]() . Erwärmen wir also einen Eisblock auf über
. Erwärmen wir also einen Eisblock auf über ![]() , beginnt dieser zu schmelzen und wird flüssig.
, beginnt dieser zu schmelzen und wird flüssig.
Der umgekehrte Vorgang von flüssig zu fest wird als Erstarren oder auch Gefrieren bezeichnet. Auch wenn es sich um die gleiche Temperatur wie beim Schmelzen handelt, wird hier manchmal vom Gefrierpunkt eines Stoffes gesprochen. Ein flüssiger Stoff gefriert dann, wenn ihm Wärme entzogen wird.
Der Gefrierpunkt von Wasser liegt ebenfalls bei ![]() , die Temperatur muss jedoch unter diesen Gefrierpunkt sinken, damit Wasser zu Eis wird. Wasser hat bei diesem Prozess noch eine Besonderheit, die sogenannte Anomalie des Wassers. Normalerweise nimmt die Dichte eines Stoffes beim Erstarren zu. Eis hat jedoch eine geringere Dichte als kaltes Wasser, wodurch es zum Beispiel auf der Oberfläche eines Sees oder des Meeres schwimmt.
, die Temperatur muss jedoch unter diesen Gefrierpunkt sinken, damit Wasser zu Eis wird. Wasser hat bei diesem Prozess noch eine Besonderheit, die sogenannte Anomalie des Wassers. Normalerweise nimmt die Dichte eines Stoffes beim Erstarren zu. Eis hat jedoch eine geringere Dichte als kaltes Wasser, wodurch es zum Beispiel auf der Oberfläche eines Sees oder des Meeres schwimmt.
Der Übergang von flüssig zu gasförmig wird Verdampfen genannt. Ein fester Stoff verdampft beim Erreichen einer bestimmten Temperatur, der sogenannten Siedetemperatur. Diese wird genau wie die Schmelztemperatur durch die Zufuhr von Wärme erreicht.
Die Siedetemperatur von Wasser liegt (bei einem Normaldruck von rund ![]() ) bei
) bei ![]() . Erwärmen wir Wasser auf über
. Erwärmen wir Wasser auf über ![]() , beginnt dieses zu verdampfen und wird gasförmig.
, beginnt dieses zu verdampfen und wird gasförmig.
Wasser kann jedoch auch schon bei kälteren Temperaturen seinen Zustand von flüssig zu gasförmig ändern. Dieser Prozess hängt mit der Luftfeuchtigkeit zusammen und wird Verdunsten genannt.
Der umgekehrte Vorgang von gasförmig zu flüssig wird Kondensieren genannt. Ein gasförmiger Stoff kondensiert dann, wenn ihm Wärme entzogen wird.
Wasserdampf kondensiert, wenn die Temperatur unter ![]() sinkt.
sinkt.
Geht ein fester Stoff direkt in den gasförmigen Zustand über, ohne vorher flüssig zu werden, sprechen wir vom Sublimieren. Auch dafür muss dem Stoff Wärme hinzugefügt werden. Der entgegengesetzte Vorgang, direkt vom gasförmigen in den festen Zustand, nennen wir Resublimieren.
Beispiele für Siede- und Schmelztemperaturen
Die folgende Tabelle zeigt die Siede- und Schmelztemperaturen von verschiedenen Stoffen sowie ihren Aggregatzustand bei Raumtemperatur. Die Angaben gelten bei Normaldruck.
| Stoff | Schmelztemperatur
in |
Siedetemperatur
in |
Aggregatzustand bei
Raumtemperatur ( |
|---|---|---|---|
| Wasser | flüssig | ||
| Sauerstoff | gasförmig | ||
| Eisen | fest | ||
| Kerzenwachs | fest |
Es ist deutlich erkennbar, dass sich die Siede- und Schmelztemperaturen stark voneinander unterscheiden. Viele Stoffe kommen in unserem Alltag nur in einem oder zwei Aggregatzuständen vor, da die Temperaturen für die Phasenübergänge nie oder nur sehr selten erreicht werden.
Häufig gestellte Fragen zum Thema Aggregatzustände









Alle Artikel aus dem Fach Physik